スイス製 医療用メッシュ MEDIFAB

透析分野など、世界で広く使用されているスイス医療向けのメッシュクロス。
医療用グレードとしてMEDIFABメッシュが存在いたします。
セミテックでもメッシュ生地単体の販売だけでなく、医療分野にMEDIFABメッシュを使用したインサート成形品を生産供給いたしております。
(※写真はイメージ画像です)
MEDIFABメッシュは下記規格がございますが製品の性質上保管管理に多くの工程を要します。
そのため即時供給は難しく海外への状況確認からのお取り寄せ品となります。
また規格品においても常時在庫体制ではございませんことご理解下さいませ。
 研究用、開発用、試験用には別途ラボパックを用意しております。
研究用、開発用、試験用には別途ラボパックを用意しております。
MEDIFABメッシュラボパックも御見積またお取り寄せとなりますが、品質確認や試験導入の際は原反生地より少量で早くお届けできるパッケージとなりますのでご利用下さいませ。
LAB PACKはご指定品番A4サイズ6枚での提供となります。
ご興味、ご要望、ご質問等ございましたら、まずはお問合せください。
MEDIFAB メッシュ LAB PACK 詳細ページへ

医療用メッシュ MEDIFABについて
医療機器産業向けのSEFAR社からの提案

MEDIFABは、医療用機器の製造時に求められる厳しい規格やクリーン度に対応するよう品質、性能のさらなる向上をはかったMEDIFAB製品が開発されました。
MEDIFABはポリエステル(PET)や、ポリアミド(PA)の単繊維(モノフィランメント)からなる化繊織物で、原料(化学繊維)は、法規(e.g.米国連邦法規集177巻21号)にしたがって生産され、生産工程は個々に認証を受け、高度の清潔さと生体適合性が保証されています。
MEDIFAB製品では、全ての規格品に対して、一般的試験の他、エンドトキシン検査及び溶血作用物質の検査が行われており、また、定期的に米国薬局方プラスチックⅣ類の検査/ISO10993の認証及び細胞傷害試験(cytotoxicitytest)が実施されています。
MEDIFABの特性

MEDIFABでは精細性、均一性を実現し、緻密なフィルタリングを実現します。
MEDIFABは保護、保持材料、フィルターとして用いられています。
たとえば点滴セット、輸血セット、血管や心臓切開時の漏出血液、血液嚢、透析装置、診断試験用ストリップなどにおいての媒体として活用されています。
※ただし、医療用機器の最終製品に用いられる全ての構成要素やSefar社製品を含む原料資材の適応性を決める事及び、機器本体の安全性と当局の規制要件などを充たす保証については医療機器製造会社の責任となります。
※MEDIFABは移植材として適用を意図したものではなく、移植材としての認可も取得されておりません。

• 一定の表面特性をもつ精密な単繊維の化繊織布です。
• 原料(化学繊維)は、米国連邦法規集(第177巻21号)及び、欧州における指針(ドイツ連邦保健庁、欧州連合 指示文書)、それぞれの規定要件を
充たしています。
• SEFAR MEDIFAB製品に関するSefar社の織布、表面仕上げの製造設備はISO9001の認証を取得しており、また、ロットの追跡可能なシステムと製造記録文書管理に関しては適応可能な"医薬品の製造管理と品質管理に関する実践規範(Good
Manufacturing Practice;GMP)"に準拠しています。
• 製造に酸素消耗性物質を用いてないこと
• エンドトキシンは低含量で0.125EU/mlよりもはるかに少ないこと
• 非溶血性であること
• 米局プラスチックⅥ類試験/ISO10993試験に適合しています
• 顧客のご要望に応じて、本来のSEFAR MEDIFABをポリエーテルエーテルケトン(PEEK)織布やポリプロピレン(PP)織布に仕上げることができます。
• 顧客要望に合わせて表面被覆加工を施すことができます
• SEFAR MEDIFABはいずれの消費でも、顧客の規格に適合させることができます
• 製造はISO14644-1によるISO7級の清浄な部屋で行われます
• 2000年版ISO9001認証の取得済みです
• ISO13485認証の取得済みです。
医療用メッシュ 規格表

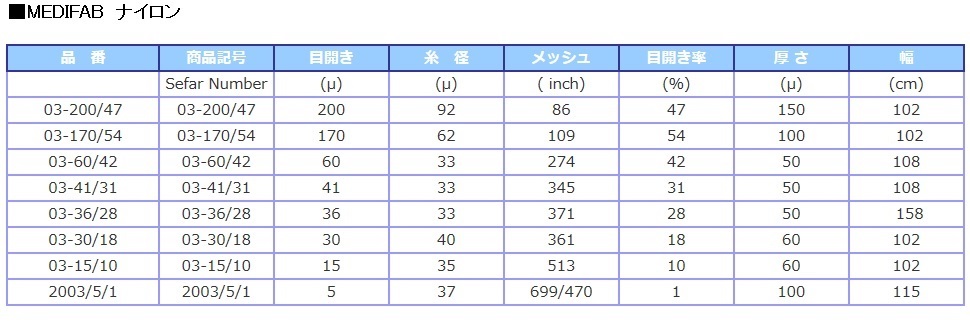
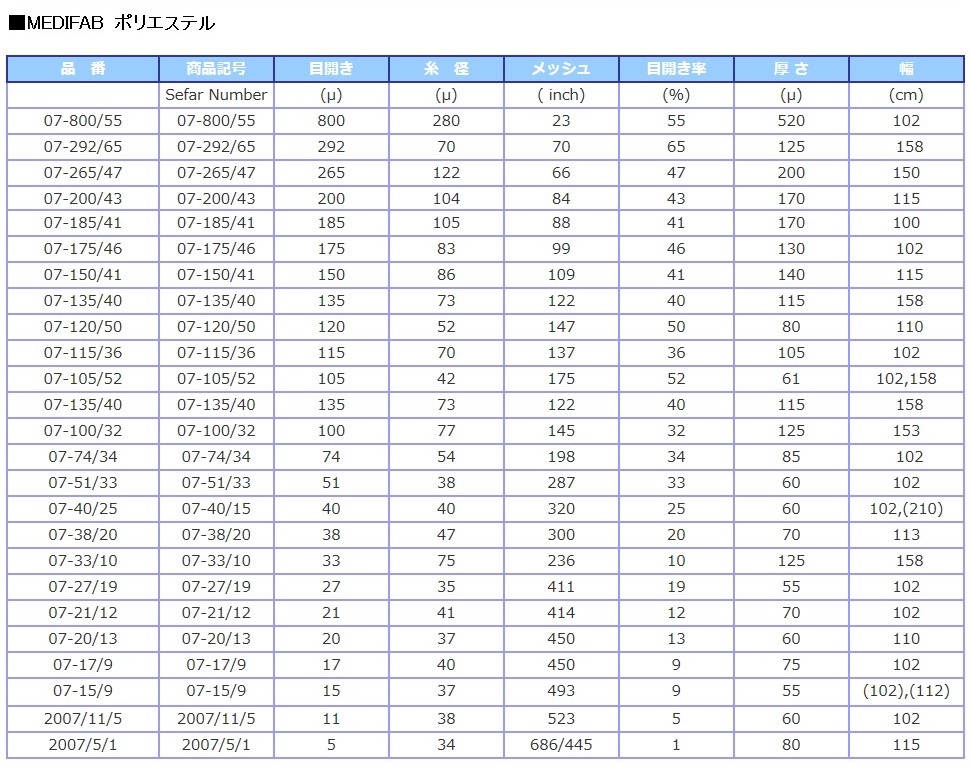
(注)規格表には国内に在庫のない物、受注生産品も記載されております。
ご入用の際は事前にお確かめください。
ご希望の規格がございましたら、1mから御見積致します。
お問合わせフォーム、もしくはFAX見積依頼シートに品番、必要m数をご記入の上ご連絡ください。 追って、回答させて頂きます。